Leyenda: el primer número es el mantenimiento y el segundo es el seguro.
Disponible en: <http://eleconomista.com.mx/finanzas-personales/2015/11/08/diversifique-sus-medios-transporte-pro-su-bolsillo>. Acceso el: 13 nov. 2015.
a) ¿Cuáles son los medios de transporte que aparecen en el gráfico?
b) Después de observar las informaciones, ¿cuál es medio de transporte que tiene menos beneficios? ¿Por qué?
c) ¿Cuál es el medio de transporte mejor para las finanzas de una persona? ¿Por qué?
Questões relacionadas
- Matemática
No círculo trigonométrico de raio unitário indicado na figura, o arco AB mede
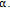 Assim, PM é igual a:
Assim, PM é igual a: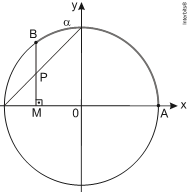
- Química | 4. Química Ambiental
(UNICAMP) Em um estudo científico, uma fina camada de um novo filtro protetor solar foi exposta previamente à radiação UVA e UVB durante diferentes intervalos de tempo, testando-se em seguida a sua eficiência em barrar essa mesma radiação. A figura a seguir mostra apenas dois dos resultados obtidos no experimento, sendo uma das curvas referente a uma exposição por 10 minutos e, a outra, a uma exposição de 30 minutos.
De acordo com essa figura, na faixa de 300 a 320 nm ao triplicar o tempo de exposição prévia, o protetor apresentou uma eficiência: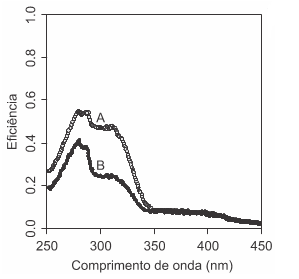
- História - Fundamental | Não Possui Tópico Definido
Observe o mapa a seguir, com as principais hidrovias brasileiras.
Embora o Brasil seja um país com abundância de rios, as hidrovias são responsáveis por apenas 14% das mercadorias transportadas. Isso ocorre porque:
- Língua Espanhola | 1.3 Modelo de Questão: ENEM X Tradicional
Por día se pierden 90000 valijas en los aeropuertos del mundo
Lo revela un informe de la Comisión Europea. Una de cada 3 000 valijas no vuelve nunca a su dueño.
En los aeropuertos del mundo se pierden, por día, unas 90 000 valijas. Así lo reveló un informe de la Comisión Europea, que censó la pérdida de 32,8 millones de maletas durante todo 2008. Si bien esto representó una baja del 20% con respecto a 2007, los expertos se muestran “preocupados” y responsabilizan del fenómeno a una multiplicidad de variables: fallas humanas y técnicas, delincuencia y el descuido personal.
“Las cifras son excesivas e inaceptables”, reconoció el comisario europeo de transporte, el italiano Antonio Tajani durante la presentación del informe, que se celebró hoy en Bruselas, Bélgica. Según el estudio, una de cada 3000 valijas extraviadas no regresan jamás a las manos de su dueño. Las aerolíneas son responsables de estas pérdidas, por las que deben pagar resarcimientos e indemnizaciones de hasta US$ 1.500, según las legislaciones.
Casi la mitad de estas fallas ocurren en vuelos con al menos una escala, resalta el documento, que elude citar los aeropuertos o compañías con mayores problemas. Por otro lado, el estudio da cuenta de otros trastornos: uno de cada 64 pasajeros no recupera su maleta tras el desembarque. Por esto, en los primeros diez meses del año pasado, 4,6 millones de equipajes fueron entregados con retraso de horas o días a sus propietarios.
“La situación es grave. Hay que intensificar los esfuerzos contra estos inconvenientes”, exclamó Tajani, quien advirtió de la necesidad de ejecutar medidas y líneas de acción para acabar con el problema. En tal sentido existe un programa de la Asociación Internacional de Transporte Aéreo (IATA) que se propone, de acá a 2012, reducir a la mitad el número de maletas perdidas.
Algunas aerolíneas, por su parte, evalúan introducir chips o sensores electrónicos en las etiquetas de identificación para controlar los movimientos de los equipajes. También se considera crear agencias nacionales, hasta ahora inexistentes, para dar un seguimiento continuo a la gestión de valijas, maletas y bolsos.
- História - Fundamental | 02. A vida familiar
As brincadeiras e a maneira de jogá-las variam de região para região no Brasil. Existem algumas brincadeiras que são comuns em estados diferentes, mas a maioria tem seu jeito próprio de brincar.
Existem as fórmulas de escolha que são brincadeiras utilizadas para escolher os participantes para um time ou mesmo para ordenar os participantes de uma determinada brincadeira. Vejamos alguns exemplos:
1) Zero ou um
Origem: Rio Branco (AC) / Jeito de brincar: Todos os participantes dizem “zero ou um” e colocam as mãos para a frente, mostrando um dedo ou nenhum. Se alguém colocar sozinho o um ou o zero, sai da brincadeira. O resto continua, até ficarem só dois participantes, que decidem a brincadeira no par ou ímpar.
2) Dedo estalado
Origem: Maranguape (CE) / Jeito de brincar:Um dos participantes coloca as mãos para trás sem que os outros vejam, e puxa os dedos de uma das mãos até que um estale. Depois, ele estica a mão para frente e cada pessoa escolhe um dedo. Quem acertar o dedo que estalou é o vencedor.
3) Senta
Origem: Cuiabá (MT) / Jeito de brincar: O grupo se reúne e alguém diz:“Quem guenta, aguenta; quem chora, senta”.E todos têm que rapidamente se sentar no chão. Quem se sentar por último será o escolhido para começar uma brincadeira.
4) Dois ou um
Origem: São Paulo (SP) / Jeito de brincar: Assim que o grupo fala “dois ou um”, todos mostram, ao mesmo tempo, um ou dois dedos. Todos os que colocam um número de dedos diferente da maioria são eliminados.
Deve-se tirar “dois ou um” até sobrar apenas duas crianças. Elas decidem quem vence no par ou ímpar.
05.1. OS BRINQUEDOS TÊM HISTÓRIA
5) Pé de chulé
Origem: Guaporé (RS) / Jeito de brincar: O grupo diz: “Pé de chulé, quem tira o seu pé?” e todos tiram o pé do chão. Quem não fizer isso será o pegador.
a) Você conhece alguma brincadeira citada? Qual?
______________________________________________________________________________________
b) Identifique no mapa o Estado que você mora com um X.
c) Coloque os números correspondentes as brincadeiras nos estados onde elas são jogadas.
www.smartkids.com.br
http://www1.folha.uol.com.br/folha/treinamento/mapadobrincar/