(Uern) Em relação às funções dos parênquimas vegetais, relacione adequadamente as colunas
| 1. Cortical. 2. Aquífero. 3. Aerífico. 4. Amilífero. | ( ) Reserva de água. ( ) Flutuação e, às vezes, respiração. ( ) Reserva de alimento. ( ) Preenchimento de espaço. |
A sequência está correta em:
Questões relacionadas
- Ciências - Fundamental | 03. Circuito Elétrico e Magnético
Texto para a questão:
Os chuveiros elétricos são aparelhos comuns nas residências brasileiras e são responsáveis por uma grande parte do consumo de energia elétrica. Por isso, é importante tomar medidas para reduzir o consumo, tanto para economizar na conta de luz quanto para contribuir com a preservação do meio ambiente. Nessa perspectiva, existem algumas práticas que podem ser adotadas para reduzir o consumo de energia elétrica ao utilizar o chuveiro elétrico.
Qual a recomendação para evitar aumento no consumo de energia elétrica ao utilizar chuveiros elétricos?
- Ciências - Fundamental | 05. Componentes Naturais
Compare as duas fotos do céu que Letícia encontrou na Internet.
Enunciado:
Complete o quadro de acordo com as fotos.
Dia ou noite? Astros visíveis
Foto 1
Foto 2
- Matemática | 12.4 Outras Funções
(FUVEST 2013 1° FASE) Uma das primeiras estimativas do raio da Terra é atribuída a Eratóstenes, estudioso grego que viveu, aproximadamente, entre 275 a.C. e 195 a.C. Sabendo que em Assuã, cidade localizada no sul do Egito, ao meio dia do solstício de verão, um bastão vertical não apresentava sombra, Eratóstenes decidiu investigar o que ocorreria, nas mesmas condições, em Alexandria, cidade no norte do Egito.
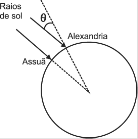
O estudioso observou que, em Alexandria, ao meio dia do solstício de verão, um bastão vertical apresentava sombra e determinou o ângulo θ entre as direções do bastão e de incidência dos raios de sol. O valor do raio da Terra, obtido a partir de θ e da distância entre Alexandria e Assuã foi de, aproximadamente, 7500 km.
Note e adote:
- Distância estimada por Eratóstenes entre Assuã e Alexandria ≈ 900 km.
- π\pi = 3
O mês em que foram realizadas as observações e o valor aproximado de θ são
- Matemática - Fundamental | 21. Problemas com as 4 Operações
Leia as ofertas de alguns produtos Harry Potter e responda o que se pede a seguir.
Débora comprou 6 cartelas de lápis. Pagou sua compra em dinheiro e recebeu o troco de R$ 13,00. Ela pagou sua compra com 2 cédulas de real. Com que notas ela pagou sua compra
- História - Fundamental | Não Possui Tópico Definido
Você se lembra do conto “A Liga dos Cabeças Vermelhas”, que leu em sala de aula? Ele mostra o detetive Sherlock Holmes desvendando um mistério. Em seu trabalho de investigação, o detetive seleciona e analisa pistas, constrói hipóteses e faz algumas deduções. Podemos comparar o método de trabalho dos detetives ao dos estudiosos que investigam o passado (arqueólogos e historiadores), pois ambos se valem de “pistas” em suas investigações.
Aponte a alternativa que contém as ações mais identificadas com o trabalho de arqueólogos e historiadores.